科研动态
当前位置:首页 >
改版2020 >
新闻中心 >
科研动态
Angew |上海药物所开发基于多酶级联反应的扁桃酸不对称合成技术
光学纯的手性扁桃酸及其衍生物是有机化学和药物化学中常用的手性拆分剂及医药中间体,应用广泛。现有的扁桃酸手性合成策略依赖过渡金属催化的不对称氢化或是有毒试剂氰化物的使用,存在反应条件苛刻、试剂昂贵和对环境不友好等缺陷。因此,开发绿色、高效、无氰化物的扁桃酸不对称合成技术具有重要意义。
针对上述问题,中国科学院上海药物研究所廖苍松团队与郑明月团队合作,设计并构建了一种基于C1延长策略的三酶级联反应和工程大肠杆菌,以苯甲醛类化合物和甘氨酸为原料,高效不对称合成扁桃酸类化合物。相关成果以“Asymmetric C1 Extension of Aldehydes through Biocatalytic Cascades for Stereodivergent Synthesis of Mandelic Acids”为题于2023年3月16日在线发表于Angew Chem Int Ed。
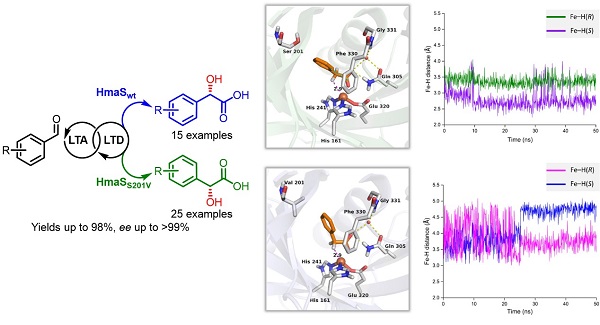
图一:三酶级联催化不对称扁桃酸合成
在本研究中,研究人员通过逆生物合成分析,设计了包含L-苯丝氨酸醛缩酶(LTA)、L-苯丝氨酸脱氨酶(LTD)和4-羟基扁桃酸合成酶(HmaS)的三酶级联反应,并通过文献和数据库挖掘,对上述酶进行了筛选,组合优化在体外构建了三酶级联反应。研究人员首次发现了HmaS催化活性口袋中关键氨基酸残基的突变体AoHmaSS201V相较于AoHmaSwt显示出对映选择性完全反转的结果,通过分子对接和分子动力学模拟实验,初步阐释了对映选择性翻转的可能酶分子机制。研究人员利用对映选择性反转的突变体,同时成功实现了S-和R-型扁桃酸类化合物的高效合成。
研究人员基于级联反应构建了工程菌株E.coli (PpLTA-RpLTD-AoHmaSwt) 和E.coli (PpLTA-RpLTD-AoHmaSS201V)作为全细胞催化剂,并优化了转化条件。全细胞反应优化过程中,团队利用芳香族氨基酸转氨酶敲除的大肠杆菌中作为底盘细胞,避免了扁桃酸合成过程中的竞争反应,提高了目标产物的转化率。最终,团队利用工程菌株催化合成15个S构型的扁桃酸类化合物(图二)及25个R构型的扁桃酸类化合物(图三),该方法显示了高收率及高立体选择性,最高产率>99%,最高ee值>99%。同时研究人员也成功实现了抗血栓药物氯吡格雷重要药物中间体(R)-邻氯扁桃酸的克级规模制备,产率为81%,ee值为98%。
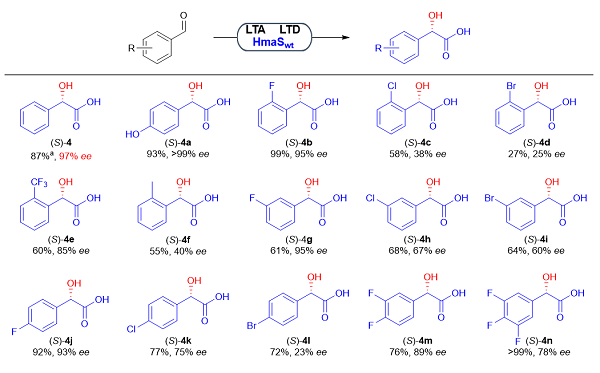
图二:三酶级联催化(S)-扁桃酸合成
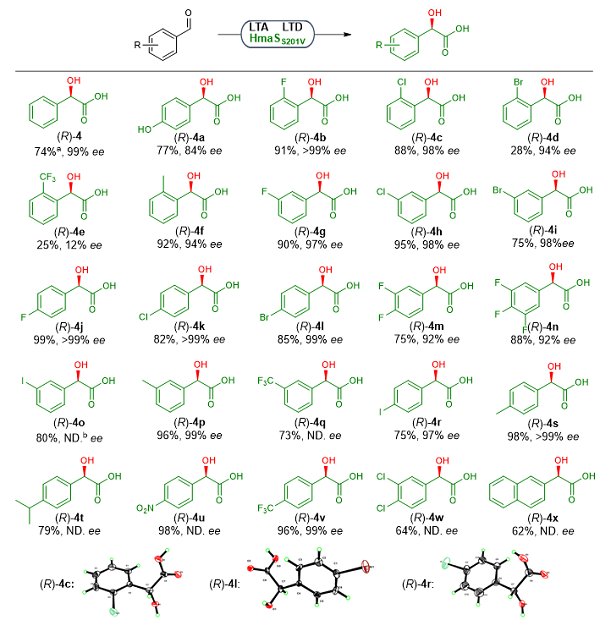
图三:三酶级联催化(R)-扁桃酸合成
通过本项研究,合作团队开发了高效的生物催化级联反应和工程菌,从易得原料苯甲醛及甘氨酸出发,以高产率和高对映选择性获得各种手性扁桃酸衍生物,该方法无需额外添加辅助因子,为扁桃酸类化合物的不对称合成提供了无氰化物的绿色生物合成新技术。
上海药物所廖苍松研究员、郑明月研究员以及廖苍松团队毛迎乐助理研究员为论文共同通讯作者,上海药物所-南京中医药大学联合培养研究生刘燕琼、上海药物所博士后付尊蕴以及研究助理董海鸿为论文第一作者。该论文得到国家自然科学基金、上海市自然科学基金、临港实验室等项目的资助。
(供稿部门:廖苍松课题组)
加强知识产权全过程管理和质量把控,专利数量、质量稳步提升,为实现创新发现的价值最大化奠定了坚实基础。2015-2019年,累计申请国内专利604件、PCT174件、国外专利402件;获得国内专利授权315件,国外专利授权176件。发明专利申请量和授权量均在国内医药行业名列前茅。
为更好地展示上海药物所成长经历,2007年药物所重建了“展示馆”,谢毓元院士为展示馆题写馆名。馆内展示主要分为“历史”和“现在”两个部分。“历尽沧桑存正道”,纵向贯穿1932年至今的药物所历史变迁;“乘势扶摇跨九天”,横向铺叙重大科研成果。展示馆先后接待国内外众多参观机构及单位,并作为上海市十个“明日科技之星”——科普拓展基地之一,接待了数千来自大中小学校的学生。