Cell Metabolism | FTO抑制剂调节肿瘤免疫逃逸抗肿瘤取得进展
中科院上海药物研究所、国科大杭州高等研究院化学生物学研究中心杨财广课题组,清华大学免疫研究所徐萌课题组和中科院北京基因组研究所韩大力课题组,在RNA去甲基化酶FTO及其小分子抑制剂调节肿瘤免疫逃逸抗肿瘤方向上的合作研究取得新进展。2021年4月27日,研究成果“Tumors exploit FTO-mediated regulation of glycolytic metabolism to evade immune surveillance”在线发表于Cell Metabolism。该研究进一步预示了小分子靶向性抑制FTO去甲基化抗肿瘤的可行性。
发展有效增强肿瘤微环境中免疫细胞抗肿瘤免疫应答的治疗策略是该研究领域的前沿方向。以组蛋白修饰为主的“表观遗传”调控基因表达在肿瘤逃避免疫监视与杀伤中发挥了重要作用,是潜在的调节肿瘤免疫抗肿瘤的新靶标。RNA去甲基化酶FTO作为“表观转录”的关键蛋白质,其抗实体肿瘤免疫的调控作用及其机制却鲜有报道。因此,研究靶向性干预FTO去甲基化功能的小分子抑制剂,具有重要的研究意义和潜在的转化价值。
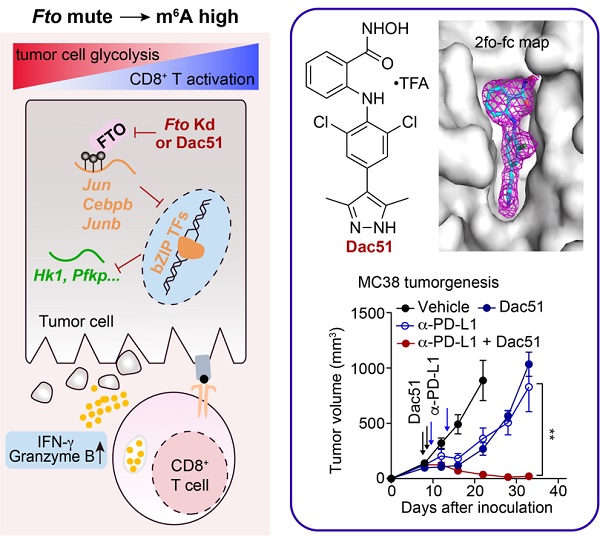
该项研究中,杨财广课题组与合作课题组共同揭示了Dac51抑制小鼠实体肿瘤细胞内FTO的去甲基化活性,提高FTO的下游靶基因bZIP家族转录因子mRNA的甲基化修饰水平,抑制糖酵解调控基因的表达,降低肿瘤细胞糖酵解水平,从而提高肿瘤浸润T细胞的免疫活性,增加干扰素和颗粒酶B等细胞因子的分泌,最终实现抑制肿瘤细胞免疫逃逸。小鼠模型上,Dac51与PD-L1单抗联用显著抑制了小鼠黑色素瘤细胞、肺癌细胞以及结肠癌细胞的成瘤性,且肿瘤完全消失的小鼠激发免疫记忆细胞应答,可抵抗10倍种植数量的小鼠结肠癌细胞的再次成瘤。该研究结果显示,FTO抑制剂Dac51能够抑制肿瘤细胞的糖代谢途径,进而增强肿瘤浸润免疫T细胞的抗肿瘤功能,具有潜在的临床应用价值。
该研究主要由清华大学、上海药物所、北京基因组研究所等单位合作完成。研究得到了国家自然科学基金委、科技部、中科院以及上海市科委等项目的资助。
上海药物所杨财广课题组较早开展RNA去甲基化酶的化学干预及其靶标成药性确证研究,已系统性发现了一批FTO的小分子抑制剂(Cell Metabolism, 2021, 33, in press; Cancer Cell, 2019, 35, 677; J. Am. Chem. Soc., 2015, 137, 13736; Nucleic Acids Res., 2015, 43, 373; J. Am. Chem. Soc., 2012, 134, 17963)。这些小分子抑制剂可以充当深入研究RNA甲基化修饰、FTO去甲基化酶的小分子工具,也将有助于推动小分子靶向RNA甲基化修饰抗肿瘤新药发现研究的新方向。
FTO抑制剂Dac51调节肿瘤免疫逃逸抗肿瘤
(供稿部门:杨财广课题组;供稿人:徐洪蛟、董泽)